提到妊娠期安全用药,大家首先想到的肯定是 ABCDX 分类法则。
1979 年,美国食品药品监督管理局(FDA)根据动物实验和临床用药经验对胎儿致畸相关的影响,建立了五级风险分类法,将药物分为 A、B、C、D、X 五类,这就是所谓的五字母系统(five-letter system),协助医生为孕妇提供安全的药物处方。

图 1 FDA 根据药物对胎儿的危害性分级
此分类看似非常简单易行,但据 FDA 收到的反馈显示:由于该分类系统过于简单,并不能反映出有效的可用信息,未能有效地传递妊娠期、哺乳期及潜在备孕男女的用药风险,常令医疗决策者感到困惑,且会导致错误的用药处方。
现有的调查和统计结果显示:
• 绝大多数女性在妊娠期至少服用过一种药物;
• 服用过 4 种或 4 种以上药物的妊娠期妇女比过去 30 年增加了 2 倍以上;
• 很多妊娠期妇女合并有慢性疾病,如哮喘、高血压、抑郁症和糖尿病,这导致她们在怀孕前仍在服用相关药物;
• 女性在妊娠期可能会出现新发疾病或原有疾病加重,需要接受药物治疗;
• 妊娠期机体各项机能会随之改变,可能会改变所需药物的剂量。
基于以上事实,FDA 希望妊娠/哺乳期女性及相关医务人员能够更加及时、有效地获取最新的药品信息,以指导妊娠期处方决策。为实现这一目的,FDA 制定了新的妊娠/哺乳期用药规则。
这一新规于 2015 年 6 月 30 日正式生效,并于近日确认最终规则(Pregnancy and Lactation Labeling Rule,PLLR or final rule)。
新规则要求:药品生产商需在其药品说明书中提供妊娠期、哺乳期妇女药物风险及获益的详细相关信息。
新修订的说明书将删除妊娠期用药五字母分级系统,针对孕妇、胎儿及哺乳期婴儿提供更多的有效信息,包括药物是否泌入乳汁、是否影响婴儿等。同时,新说明书还将加入 「备孕的男性与女性」条目,就药物对妊娠测试、避孕及生育的影响注明相关信息。
新修订后的说明书将包括以下信息:
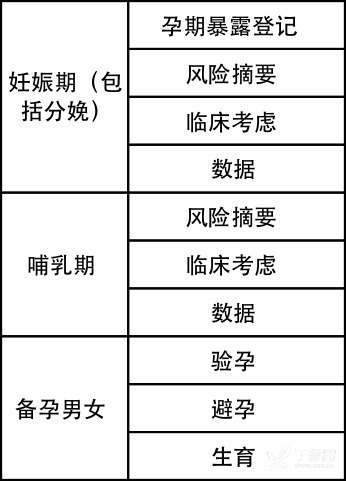
除此之外,新说明书还将包括孕期药物暴露、药物疗效信息收集与上报登记系统,鼓励正在服用药物或生物制品的孕妇将相关信息上报参与研究。
修订后的说明书将会改变原有的诊疗状况,医生能获得及时更新、且归纳总结过的妊娠期哺乳期相关药物信息。但新规则并不覆盖非处方药物(OTC),OTC 的妊娠/哺乳期用药指导暂不会改变。
由于 FDA 要求所有制药公司在说明书中删除妊娠期字母分类,并根据更新信息及时修订说明书。这项浩大的工程可能会持续数年之久。但数千种药物根据最新的科学信息修订说明书,将有更加完善的描述信息,患者将是最大的受益者,也让医务人员及患者对治疗用药更有信心。
参考文献:
https://www.fda.gov/Drugs/DevelopmentApprovalProcess/DevelopmentResources/Labeling/ucm093307.htm
https://www.drugs.com/pregnancy-categories.html
